Las Enfermedades Monogénicas y Poligénicas: “El Efecto Mariposa desde Nuestros Genes”
Por Aleph Prieto Moreno
Revisión en divulgación: M. en C. Alma Mendoza Ponce
Revisión en Fidelidad Científica: Dr. Víctor Rosales Salyano
"Nadie puede arrancar una flor sin perturbar una estrella"
Nezahualcóyotl
¿Quién de nosotros no ha sufrido las inclemencias del clima? Para algunas personas atender el reporte meteorológico por las mañanas se ha convertido en parte de la agenda del día: sales de tu casa con tu mejor abrigo y tu paraguas, tomando en cuenta las recomendaciones de la atractiva mujer que da el reporte meteorológico cuando a medio día, con un calor endemoniado que te hace sudar como puberto en primera cita y te das cuenta que debiste haberte puesto más desodorante. Un mal pronóstico del clima nos puede dejar tirados en las peores circunstancias con un calor, lluvia o frío extremosos, lo que nos lleva a preguntarnos por qué caramba confiamos en el pronóstico del tiempo. Es un hecho: algunas veces los reportes del clima se equivocan; sin embrago, debemos darles más crédito. A decir verdad, predicen correctamente el clima la mayor parte de las veces para periodos cortos, como horas y días. Y es que el clima se concibe como un sistema complejo en el que influyen muchos factores. Esto lo sabía perfectamente el meteorólogo Edward Lorenz, quien tomó especial atención en factores como la humedad y la temperatura, a partir de las cuales se puede conocer la manera en la que cambian tanto la temperatura como la velocidad del aire a lo largo del tiempo. Lorenz, a través de un modelo matemático y del conocimiento de las condiciones iniciales en el comportamiento de la atmósfera generó predicciones climatológicas. Su modelo simulaba, según las condiciones establecidas, el estado futuro cercano de la atmósfera pudiendo así conocer el clima del día siguiente. Sin embargo, con gran sorpresa, Lorenz observó que su modelo era muy sensible a las condiciones iniciales; pequeñas diferencias en los datos de partida (algo aparentemente tan simple como variar un decimal en los datos de la temperatura o la humedad) llevaba a grandes diferencias en las predicciones que el modelo generaba.

El principal problema en la predicción del clima se debe a que no se conocen por completo las variables que afectan la evolución de la atmósfera ni los cambios en las condiciones iniciales de este sistema natural. La evolución del clima, como ya se ha comentado, es un sistema muy sensible a las condiciones iniciales: su estado futuro depende significativamente de su partida, del estado actual o inicial. Si partimos de una atmósfera cuyo estado inicial no es perfectamente conocido, tendremos que tener en mente que la evolución de la “atmósfera” que analiza el modelo será diferente, y ya desde un principio lo es, a la real. En un ejemplo hipotético, extremista y exagerado, si las condiciones iniciales no contemplan el simple aleteo de una mariposa en una región del planeta, el modelo podría llevar a un grave error en las predicciones: de aquí la famosa frase “El aleteo de una mariposa en Hong Kong puede desatar una tormenta en Nueva York”. El “efecto mariposa”, como Lorenz lo llamó, se refiere a la alteración amplificada de un resultado debido a la variación de las condiciones iniciales en un sistema natural complejo. En otras palabras, cualquier pequeña perturbación o variación en las condiciones iniciales de un sistema complejo puede generar que éste evolucione en formas totalmente diferentes: cambia las condiciones iniciales y lo cambiarás todo.
En la vida de los seres humanos, como de cualquier organismo, los genes forman parte de las condiciones iniciales de su evolución. Los genes son como una receta, es decir, las instrucciones que indican el orden y el tipo de aminoácidos que conformaran una determinada proteína. La importancia de sintetizar proteínas es mucha, ya que estas biomoléculas realizan diferentes funciones: catalizan reacciones químicas (enzimas), participan en la comunicación celular (receptores y hormonas), en el transporte (hemoglobina), en la defensa del organismo (anticuerpos) y forman parte de los componentes estructurales de células y tejidos. La función de una proteína está determinada en gran parte por su estructura, la cual depende de la secuencia de aminoácidos que la conforman que, como habíamos mencionado, está inscrita en el gen (receta) correspondiente. Por lo tanto, cualquier cambio en un gen puede modificar la estructura de la proteína que codifica, alterar su función y, como consecuencia, afectar un proceso fisiológico. Lo anterior puede ser el origen de una enfermedad... cambia un fragmento del DNA de un ser humano y cambiarás su destino.
El más puro determinismo genético: las enfermedades monogénicas
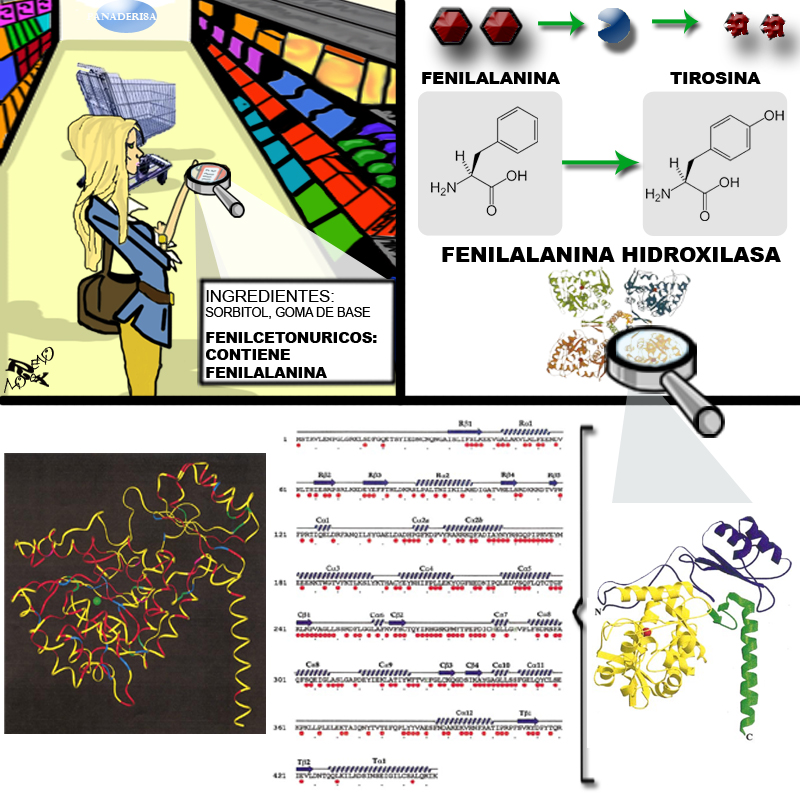
“Contiene fenilalanina”. Es probable que recuerdes haber leído esta frase. Aunque para la mayoría de las personas no tenga mucha importancia, esta nota de advertencia inscrita en algunos productos alimenticios deben de tomarla muy en serio las personas que padecen Fenilcetonuria. Los pacientes afectados por esta enfermedad tienen un defecto en la enzima llamada fenilalanina hidroxilasa(PAH), que participa en el metabolismo del aminoácido fenilalanina. La fenilalanina juega un papel importante en la producción de melanina, el pigmento responsable del color de la piel y del cabello; por lo tanto, las personas con esta enfermedad usualmente tienen un cutis, cabello y ojos más claros que quienes no la padecemos. Si las personas con Fenilcetonuria no evitan los alimentos que contienen fenilalanina, al no ser transformado adecuadamente por la enzima fenilalanina hidroxilasa, este aminoácido y dos substancias estrechamente relacionadas se acumulan en el cuerpo. Cuando se incrementan los niveles de estas sustancias, se vuelven dañinas para el sistema nervioso central y ocasionan daño cerebral en los fenilcetonúricos.
Además de heredarnos los rasgos físicos, nuestros progenitores nos transmiten también la predisposición a desarrollar determinados padecimientos, ambas cosas a través de los genes. El primero en sugerir que en las enfermedades congénitas se hereda un factor -ahora lo llamamos gen-, que produce una proteína que funciona mal, fue un médico británico llamado Archibald Garrod. En 1910, Garrod observó que el mal llamado Alcaptonuria se transmitía de padres a hijos de manera recesiva, es decir, esta enfermedad se presenta únicamente en caso de que se herede el mismo “error” de cada progenitor (De igual forma se hereda la Fenilcetonuria). Los pacientes con Alcaptonuria presentan artritis y, dependiendo de su dieta, la orina y la cera de sus oídos se tornan rojizas o negras cuando se exponen al aire. Dicha coloración se debe a un aumento en la cantidad de una sustancia conocida como ácido homogentísico. Garrod supuso que este compuesto era un producto normal de la química del cuerpo que, en las personas sanas, era transformado en otra sustancia antes de eliminarse. Por lo tanto, Garrod dedujo que la Alcaptonuria se desarrollaba debido a la pérdida o mal funcionamiento de una proteína que actuaba como catalizador en la transformación química de ácido homogentísico. Actualmente sabemos que esta proteína es una enzima llamada ácido homogentísico oxidasa y que en los enfermos de Alcaptonuria dicha enzima existe, pero no funciona adecuadamente. El defecto en la enzima se debe a un cambio en las instrucciones para sintetizarla, un cambio en la secuencia del gen que la codifica.
En las últimas dos décadas se ha vuelto muy común escuchar que existen genes asociados con enfermedades. Sin embargo, lo que los científicos reportan es la asociación de ciertos “errores” en un determinado gen con el desarrollo de algún padecimiento. No hay genes de la enfermedad de Parkinson o de la esquizofrenia, pero en cambio existen ciertas variantes de algunos genes que se presentan con mayor frecuencia en estos pacientes que en las personas sanas. A partir de las investigaciones de Garrod se piensa que la proteína, producto de una de estas variantes genéticas, altera algún proceso fisiológico y de esta manera incrementa la susceptibilidad de las personas a desarrollar un determinado padecimiento o en algunos casos, es la causa del mismo. En pocas palabras, todos tenemos el gen “involucrado”, pero los pacientes tienen una variante que contiene un “error”, un cambio en la secuencia. El cambio de un nucleótido por otro es una mutación que, cuando se presenta en más del 5% de la población, se le conoce como polimorfismo de un solo nucleótido o SNP (del inglés Single Nucleotide Polymorphism). En algunos casos, la herencia de un solo “error” en un único gen lleva a una enfermedad. Debido a su origen, estas enfermedades son llamadas monogénicas. Tal es el caso de la Fenilcetonuria y de la Anemia falciforme, esta última originada por un defecto en el gen de la hemoglobina. También es una enfermedad monogénica la Inmunodeficiencia Severa Combinada, un padecimiento que deja sin defensas a las personas que presentan una mutación en el gen que codifica para la adenosina desaminasa, una enzima que participa en la generación de células del sistema inmune (linfocitos).
El Huntington como otra enfermedad monogénica: “Un genoma tartamudo”
“No recuerdo la apariencia de las personas después de conocerlas. En los últimos dos años me he caído un par de veces. Si tengo prisa, tropiezo. Se me caen las cosas;no tengo ningún sentido del ritmo; por lo tanto ya no puedo bailar, me muevo nerviosamente. Cuando miro el reloj inmediatamente olvido qué hora marcaba; antes era capaz de valorar lo que eran 5 minutos o media hora, ahora me levanto por la mañana y antes de que me de cuenta es hora de irse a la cama - ¡el tiempo vuela!
Éstas son algunas de las tantas experiencias que sufren las personas que padecen la enfermedad de Huntington. La aparición de una enfermedad como ésta puede ser tan dramáticamente predeterminada sólo por cambios o mutaciones en el DNA. Las mutaciones pueden ir desde la simple sustitución de una de las cuatro bases nitrogenadas que lo conforman (adenina = A, guanina = G, timina = T, citosina = C) hasta la remoción o la adición de un fragmento largo de la doble hélice, ¡literalmente cachos del DNA! Esto último es lo que ocurre con la huntingtina, la proteína clave en la enfermedad de Huntington. Para describir qué tienen que ver los genes en la enfermedad de Huntington repasemos brevemente la manera en que un gen codifica para una proteína. La analogía del genoma como un libro nos será muy útil: cada base (A, T, C, G) en el DNA es una letra que, de acuerdo con el código genético, forma palabras de tres letras que corresponden a los aminoácidos; al unir las palabras en oraciones formamos proteínas. En los pacientes con Huntington, a la mitad de la secuencia del gen que codifica para la huntingtina se repite la “palabra” CAG (esta secuencia de tres letras CAG codifica para el aminoácido glutamina), lo que produce un tramo largo de glutaminas en mitad de la proteína. La “palabra” se repite una y otra vez: CAG, CAG, CAG, CAG, CAG… puede repetirse seis, 30 o incluso más de 100 veces; ésta es la condición inicial. Si la palabra se repite 39 veces o más, a mediana edad el individuo comenzará a sufrir un deterioro de las facultades intelectuales seguido de espasmos en las extremidades, depresión profunda y alucinaciones, lo que en conjunto llevará a una muerte prematura, debida principalmente a la incapacidad que todos estos factores originan. Entre mayor sea el número de repeticiones, a más temprana edad iniciará la demencia: en promedio, los que tienen 39 repeticiones iniciarán con los síntomas a los 66 años, mientras que los que tienen 50 repeticiones de la “palabra” perderán la cabeza aproximadamente a los 27 años. A diferencia de la Alcaptonuria, la enfermedad de Huntington es una enfermedad genética dominante, esto significa que basta con una sola copia del gen mutante proveniente de la madre o del padre para desarrollar la enfermedad. En 1993 se identificó el gen y la mutación que llevan a la enfermedad; sin embargo, a la fecha no queda claro el mecanismo que relaciona la mutación con la patología característica de estos pacientes. Muchas evidencias al respecto sugieren que el aumento en el número de glutaminas en la huntingtina afecta su plegado tridimensional normal; es decir su forma en el ambiente celular. De esta forma, un cambio en la estructura de esta proteína genera la acumulación de agregados proteicos que causan la muerte de un tipo particular de neuronas en el cerebro de estos pacientes.
Un sistema complejo de verdad: las enfermedades poligénicas
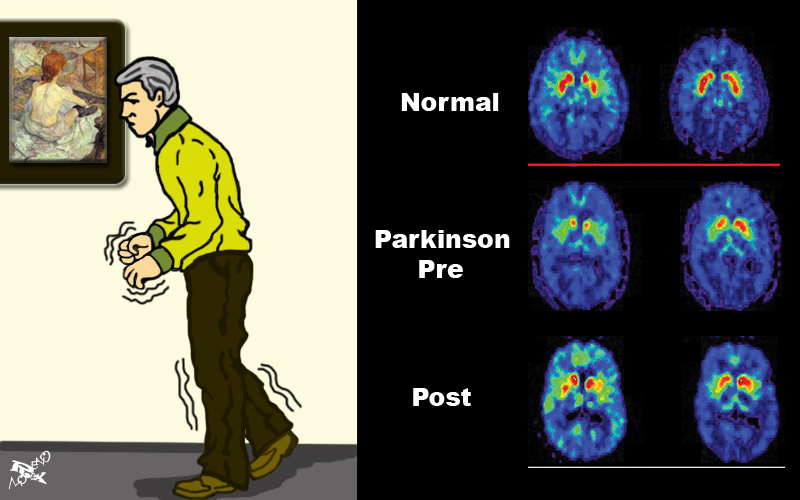
Haciendo una analogía, puede decirse que las enfermedades monogénicas pueden verse como las tonalidades en una fotografía blanco el negro, o como los ceros y unos del lenguaje digital: “tienes la mutación, tienes la enfermedad; o no tienes ni una ni otra”. Sin embargo, existen los matices, la escala de grises, los “depende”, y en la mayoría de las enfermedades ocurre un fenómeno conocido como “pleiotropía”, término que alude a los efectos de muchos genes para desencadenar una patología. Tal es el caso de la enfermedad de Parkinson, un padecimiento neurodegenerativo que se manifiesta por lo general en personas de edad avanzada y que se caracteriza por la muerte de las neuronas de una región del cerebro llamada sustancia negra. Normalmente estas neuronas producen dopamina, un neuromodulador que regula las señales a través de las cuales se comunican las neuronas. En la enfermedad de Parkinson, la pérdida de estas neuronas está asociada con un conjunto de cambios genéticos que derivan en el enfermo en lentitud de movimientos voluntarios (bradicinesia), ausencia de movimiento (acinesia), rigidez muscular y temblores. Nos enfocaremos en este último rasgo, conocido como “temblor esencial”, que puede presentarse individualmente o como uno de los signos del Parkinson.
¿Alguna vez has temblado? Seguro que sí, ¿recuerdas qué ocasionó el temblor? Todas las personas conocemos el temblor, una manifestación fisiológica que experimentamos cuando sentimos miedo, cuando estamos muy nerviosos, cuando tenemos mucho frío o cuando después de una borrachera amanecemos “crudos”. Factores de origen no genético como el estrés, la fatiga, los corajes, la cafeína, el cigarrillo y algunas drogas, pueden intensificar temporalmente algunos de estos temblores. Sin embargo, en algunos individuos los temblores se tornan más frecuentes que en el promedio de la población debido a factores genéticos. En estos casos se trata del temblor esencial, que se caracteriza por movimientos involuntarios de las extremidades. Esta afección fue descrita en personajes históricos, tales como Adolfo Hitler; los más íntimos colaboradores y secretarias del “führer” se percataron de este temblor esencial como parte del Parkinson que sufría a sus 50 años de vida.
A principios de la década de 1960, los investigadores identificaron que en los pacientes con Parkinson, tras la pérdida de las neuronas de la sustancia negra, disminuían de manera crónica los niveles de dopamina en el cerebro. En el sistema nervioso, la dopamina cumple sus funciones al activar a sus receptores. Recientemente se describió que el cambio de una adenina (A) por una guanina (G) en la secuencia del gen del receptor tipo 3 de dopamina (DR3) juega un papel importante en el Temblor esencial. Lo anterior fue sugerido al encontrar que esta mutación (A → G) se presenta con mayor frecuencia en los pacientes con Temblor esencial que en los sujetos sanos.
El D3R participa en el control de los movimientos voluntarios. De manera interesante, se encontró que el DR3 mutante era más eficiente para realizar algunas de sus funciones que el D3R de los sujetos sanos. Vale la pena resaltar esto último, ya que ilustra que los cambios en los genes que pueden predisponer a una persona a padecer alguna enfermedad no son solamente mutaciones que afectan negativamente la función de la proteína correspondiente. También, es oportuno observar que lo que encontró el estudio referido, y que sitúa a la mutación del DR3 como un factor importante en el desarrollo de Temblor esencial, es su elevada presencia en los pacientes con dicha enfermedad. No obstante, no todos los pacientes con Temblor esencial presentaron la mutación, y más aún, la mutación se encontró en algunos sujetos sanos. Esto sugiere que si bien la mutación descrita del gen del DR3 está involucrada en la susceptibilidad de padecer temblor esencial, otros factores juegan también un papel importante. Estos factores pueden ser variantes en otros genes. Esta cuestión se hace más importante cuando tratamos de entender las causas genéticas del Parkinson, donde el Temblor esencial sólo nos permite entender uno de sus componentes. En las enfermedades poligénicas, como su nombre lo indica, deben presentarse cambios en la secuencia de muchos genes. Una sola mutación es, en algunos casos, insuficiente (sujetos sanos con la mutación), y en otros, innecesaria para inducir la enfermedad de un padecimiento (pacientes sin la mutación).
Es claro entonces que en el caso de las enfermedades poligénicas la herencia de una mutación no lleva directamente a la enfermedad, en realidad la presencia de sólo un error nos hace más susceptibles a desarrollar cierto padecimiento. Esto sugiere que existen factores que pueden anular el efecto que tiene dicha mutación; sin embargo, si alguno de estos factores “anuladores” también presenta defectos, entonces la susceptibilidad aumenta. Ahora, si consideramos que la participación de los genes es, a lo mucho, una parte del cuento que se completa al incluir la influencia de los factores ambientales, entonces el cuadro se vuelve más complejo, pero también más real. Éste sería el caso de enfermedades tan complicadas como la Diabetes y el Cáncer, en las cuales la búsqueda de variantes génicas presentes preferentemente en los pacientes empieza a arrojar resultados prometedores, que permitirán mejorar el diagnóstico, fortalecer la prevención y, no menos importante, entender con mayor claridad los mecanismos patológicos que conducen a la enfermedad.
En este punto, es importante aclarar al lector que no todos los cambios en las secuencias del DNA derivan en enfermedades o incluso en alteraciones que podrían traer algún beneficio para el organismo. De hecho, se ha encontrado que la mayor parte de los cambios en los genomas (mutaciones en el DNA) no producen ningún efecto positivo ni negativo directo en el organismo, es decir, pueden ser consideradas mutaciones neutrales; esto convierte a los investigadores en detectives entrenados para encontrar en los genomas las mutaciones que sí participan en el desencadenamiento de un cambio fisiológico importante para el organismo.
El efecto mariposa en nuestro destino
Como se había mencionado, en el efecto mariposa un cambio en las condiciones iniciales tiene una gran influencia en el resultado final. Citemos aquí otra de las características del efecto mariposa: “las mismas condiciones iniciales siempre conducen al mismo resultado”. Esto nos dice que si conocemos la genética de un individuo, por ejemplo el número de repeticiones CAG del gen de la huntingtina, es posible predecir con bastante seguridad parte del desenlace fisiológico de su vida. En el caso de la enfermedad de Huntington -y en general en todas las enfermedades monogénicas- es sorprendente la exactitud con que unas cuantas “palabras”-o incluso “letras”- insertadas en los mil millones de “palabras de tres letras” del genoma sean la diferencia entre la cordura y la demencia, entre la salud y la enfermedad. En el caso de las enfermedades poligénicas, en las cuales se requiere de la presencia de “errores” en diferentes genes, se puede llegar al mismo resultado mediante diferentes combinaciones de muchas variables, que incluyen genes y factores ambientales. Al considerar todas las variables como las condiciones iniciales tenemos entonces un sistema caótico cuyo desenlace es, de acuerdo con los matemáticos, impredecible pero determinista.
Los avances científicos de las últimas décadas han hecho posible tener acceso a la información presente en el genoma. Esto, además de su valor per se, ha resultado útil en el diagnóstico de muchas enfermedades. En los casos más alentadores, analizar nuestros genes nos ha permitido prevenir ciertos padecimientos con tan sólo la modificación de algunos aspectos de nuestro estilo de vida. Por ejemplo, en enfermedades monogénicas como los errores innatos del metabolismo (entre éstos la alcaptonuria y la fenilcetonuria) al eliminar de la dieta los compuestos que no pueden ser degradados se soluciona el problema. Algo similar se aplicaría para las personas genéticamente susceptibles a la diabetes. A esto se le conoce como medicina preventiva, y recientemente ha ganado importancia debido a que se podría retrasar, o en algunos casos evitar el desarrollo de ciertos padecimientos. Lo anterior no sólo traería una reducción en el costo del tratamiento correspondiente, sino también significaría una mejor calidad de vida para la población. Sin embargo, aún falta mucho por hacer, y en padecimientos como la enfermedad de Huntington, conocer nuestros genes sólo nos puede dar información, pero todavía no nos permite encontrar el remedio correspondiente. Por el momento, el análisis del genoma en estos casos únicamente nos da la clase más desoladora de autoconocimiento: el conocimiento de nuestro destino.
Esta limitación del conocimiento científico no es exclusiva de las Ciencias Genómicas, ya que puede ser trasladada directamente al fenómeno del clima. Incluso con los medios que disponemos hoy en día (satélites, radares, estaciones automáticas de superficie, datos de sondeo, etc.) el conocimiento del estado inicial de la atmósfera es limitado en el tiempo y en el espacio; lo cual repercute en la predictibilidad del clima. Las observaciones son puntuales, discretas y no cubren a toda la Tierra. Además, muchos datos están provistos de errores que deben ser tratados, eliminados, depurados, etc. Por todos estos motivos, el estado de partida del conocimiento de la atmósfera es incompleto y discreto. Por lo tanto, debido a que la calidad y cantidad de los datos de partida de un modelo natural, como el clima, son críticas para la fiabilidad de las predicciones futuras, una de las motivaciones más importantes de las Ciencias Genómicas la constituye conocer mejor las condiciones iniciales de un genoma determinado. Lo anterior nos puede permitir conocer las características que determinan el buen o mal funcionamiento de un organismo, esto con el fin de que las predicciones sobre la evolución de estos mecanismos sean las más acertadas. Tal vez algún día con sólo poseer la información necesaria de nuestro genoma podamos tener una historia de vida con igual o mayor certeza con la que ahora disfrutamos de la lluvia o de un día soleado.
Agradecimientos:
A la M. en C. Irma Lozada Chávez por la revisión crítica de este documento y, de manera particular, por sus valiosas sugerencias.
Biografía del autor:
Aleph Prieto Moreno es químico farmacéutico-biológico de profesión y divulgador de la ciencia, terminó la Maestría en Ciencias Bioquímicas en el 2005 en la UNAM Actualmente imparte la asignatura de Bioquímica en la Facultad de Química de la UNAM y se encuentra cursando el Doctorado en Ciencias Bioquímicas en el Departamento de Biofísica del Instituto de Fisiología Celular también de la UNAM. Sus principales áreas de investigación se enfocan en los mecanismos involucrados en la modulación de la actividad neuronal.
Comentarios a: aleph@ifc.unam.mx
Bibliografía:
-
- Ridley M. Genoma. La autobiografía de una especia en 23 capítulos. México, Ed. Taurus, 2001.
- Mondragón M. El determinismo genético. ¿Cómo ves? No.10, p. 8.
- Jeanneteau F., et al. A functional variant of the dopamine D3 receptor is associated with risk and age-at-onset of essential tremor. Proc Natl Acad Sci U S A. 2006; 103(28):10753-8.
- Eisensmith RC, Woo SL. Molecular basis of phenylketonuria and related hyperphenylalaninemias: mutations and polymorphisms in the human phenylalanine hydroxylase gene. Hum Mutat. 1992;1(1):13-23.
